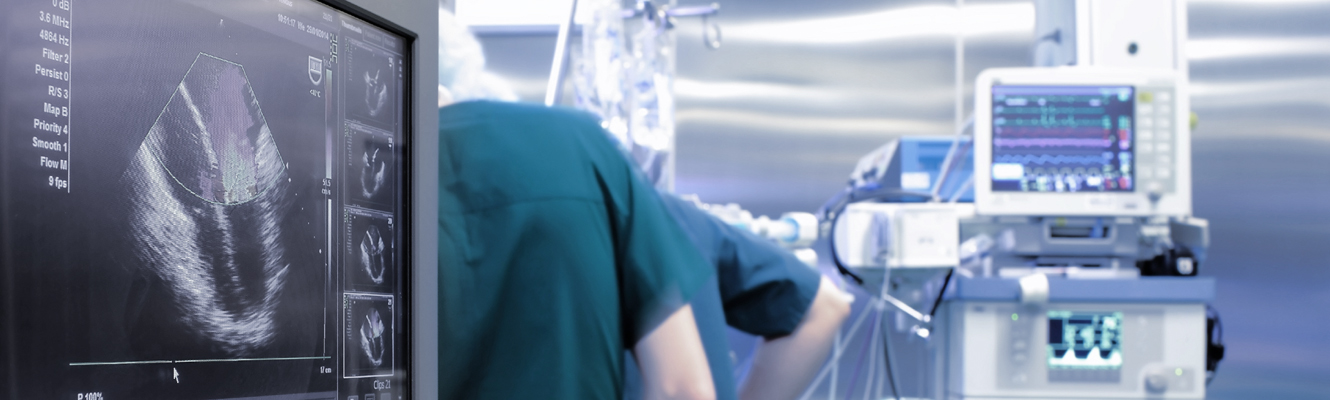
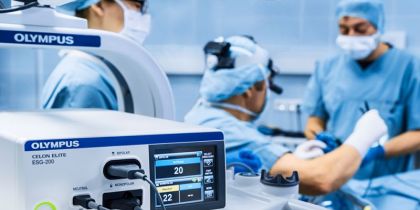
Medical Technology
Softwarebasierte Anwendungen im Bereich Medizintechnik sind im Allgemeinen medizinische Geräte der Informationstechnologie, Biotechnologie und Gesundheitsdienstleistungen, es kommen aber auch Mobile Medical Applications (Apps) als Medizinprodukte zum Einsatz.
Der Begriff Medizintechnik 4.0 hat sich für vernetzte Medizingeräte, die ihre diagnostischen und therapeutischen Eigenschaften und Funktionen über programmierbare Anwendungsschnittstellen (APIs – „Application Programming Interfaces“) und über digitale Dienste (Services) austauschen, etabliert.
Im Bereich Medizintechnik werden des Weiteren auch prozessunterstützende Software Werkzeuge, die potenziell Einfluss auf die Produktqualität haben können, eingesetzt.
In diesen sicherheitskritischen Themenbereichen gilt, dass für diese Produkte die normenkonforme Entwicklung je nach Einsatz nachgewiesen werden muss. Entsprechend hoch sind zum Beispiel die Anforderungen der IEC 62304 an die Entwicklung. Bei den Entwicklungsprozessen stehen vor allem das Risikomanagement, die Gebrauchstauglichkeit und Rückverfolgbarkeit im Fokus. In diesem Umfeld müssen auch die Anforderungen zum Qualitätsmanagement aus der EN ISO 13485 erfüllt werden.
Prozess-, Kritikalitäts- und Part-11-Compliance-Analysen können dabei den zu prüfenden Funktionsumfang und Testabläufe festlegen.
Normenkonformität
Wir arbeiten u.a. nach folgenden Normen
- DIN EN ISO 13485 „ Medizinprodukte – Qualitätsmanagementsysteme – Anforderungen für regulatorische Zwecke
- FDA 21CFR 820 Quality system regulations
- FDA 21 CFR Part 11 Electronic Records; Electronic Signatures (ERES)
- IEC 62304 – medical device software – software life cycle processes
- DIN EN ISO 14971 Medizinprodukte – Anwendung des Risikomanagements auf Medizinprodukte
Code Review inkl. statischer Code Analyse von IEC62304 konformer Software
Die IEC 62304 (Medizingeräte-Software – Software-Lebenszyklus-Prozesse) fordert nicht explizit, dass ein Code-Review durchgeführt werden muss. Wir empfehlen jedoch auf Basis der Sicherheitsklassifizierung für sicherheitskritische Teile der Sicherheitsklasse C und für komplexe Module Reviews mit dem Ziel durchzuführen, die Abdeckung der Requirement- und Design-Vorgaben durch die Softwaremodule nachzuweisen.
Darüber hinaus erhöht sich die Qualität der Software messbar durch Code-Coverage-Analysen, die die unterschiedlichen Abdeckungsgrade des Codes durch Tests und Reviews analysieren und die Traceability zu den Testfällen überprüfen. Worst-Case Laufzeit Analyse (WCET-Analyse) und Floating Point Error Analyse sind weitere Verfahren, die herangezogen werden können, um die Qualität des Codes zu erhöhen bzw. nachzuweisen. Selbstverständlich berücksichtigen wir bei den Code-Coverage-Analysen auch Ihre internen Coding-Standards.
Software-Entwicklungsprozess
Wir unterstützen Sie als Dienstleister in allen Phasen Ihres Software-Entwicklungsprozesses. Unsere Mitarbeiter haben große Erfahrung in allen Bereichen rund um das Thema Software-Entwicklungsprozess für Ihre medizintechnisch-spezifischen Anwendungen, unter Berücksichtigung der IEC 62304 und abgestimmt auf die Sicherheitsklasse, beginnend mit dem Aufstellen von Anforderungen (Requirement Engineering), über die Definition von geeigneten Architekturen und Designs, Sourcecode-Analysen, den verschiedenen Teststufen bis hin zur Ausarbeitung einer geeigneten Verifikations- und Validierungsstrategie. Dabei ist es für uns nicht relevant, ob ihr Entwicklungsprozess auf dem Wasserfall-Modell, dem V-Modell oder auf einem agilen Entwicklungs-Ansatz (z.B. SCRUM) aufsetzt.
Verifikation und Validierung
Speziell in den Bereichen Verifikation und Validierung sind wir Ihr kompetenter Ansprechpartner. Durch unsere jahrelangen Projekterfahrungen in der Verifikation und Validierung von diversen medizintechnisch-spezifischen Anwendungen und prozessunterstützender Software Werkzeuge können wir gemeinsam mit Ihnen die optimale Verifikations- und Validierungs-Vorgehensweise erstellen und Sie bei der Umsetzung innerhalb der Projekte praktisch unterstützen. Dabei stehen für uns immer Aufwand und regulatorische Notwendigkeit im Fokus.
Referenzprojekt
Ein Medizintechnikhersteller führte ein neues Dokumenten-Lifecycle-System ein. Hierzu wurde das Tool Agile als Engineering Backbone in der Entwicklung und Produktion eingesetzt und kontinuierlich weiterentwickelt. Es wurden u.a. Schnittstellen zu SAP, CAD-Systemen und MS Office implementiert. Da es sich um prozessunterstützende Software handelt, die potenziell Einfluss auf die Produktqualität haben könnte, führte die certitudo GmbH qualitätssichernde Maßnahmen gemäß FDA 21 CFR Part 11 durch.
Zu den ausgeführten Tätigkeiten gehörten
- Erstellung von Anforderungsdokumenten
- Erstellung von Testspezifikationen
- Erstellung von Risikoanalysen
- Aufbau der Validierungsdokumentation und einer automatischen Traceabilitymatrix
- Ausführung von manuellen Systemtests
- Entwicklung eines Testroboters für automatische Funktionstests
- Erstellung von Handbüchern und elektronischen Tutorials